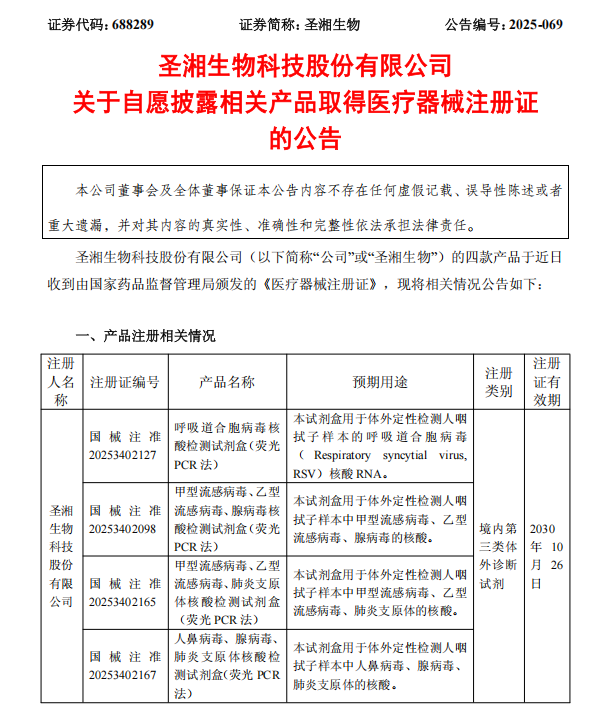
2025年11月1日,圣湘生物科技股份有限公司(证券代码:688289,以下简称“圣湘生物”)发布公告,自愿披露其四款呼吸道病原体核酸检测试剂盒获国家药品监督管理局批准,取得医疗器械注册证。这四款产品均采用荧光PCR技术,涵盖六种常见呼吸道病原体,进一步丰富了公司“小联检”产品线,提升了在呼吸道感染诊断领域的综合竞争力。
产品详情与技术特点
本次获批的四款试剂盒具体包括:
呼吸道合胞病毒核酸检测试剂盒
甲型流感病毒、乙型流感病毒、腺病毒核酸检测试剂盒
甲型流感病毒、乙型流感病毒、肺炎支原体核酸检测试剂盒
人鼻病毒、腺病毒、肺炎支原体核酸检测试剂盒
近日,全国呼吸道感染疫情呈上升趋势,托幼机构、中小学聚集性疫情频发。中国疾控中心最新监测数据显示:鼻病毒检出率高达12.8%,流感病毒、呼吸道合胞病毒(RSV)均处于活跃流行期。在此背景下,圣湘生物“四证连发”的战略意义不言而喻。其新获批的四款试剂盒精准覆盖北京市卫健委推荐的六大核心靶标——甲流、乙流、RSV、鼻病毒、腺病毒、肺炎支原体,堪称“直击临床痛点”。与传统单一检测相比,圣湘此次推出的“小联检”系列具备三大颠覆性优势:1. 速度革命:最快30分钟完成精准鉴别,契合门急诊“随到随检”需求2. 技术升级:多重荧光PCR技术+专利超声直扩方案,实现“免提取、闭管检测”3. 灵活组合:支持根据地域、季节、人群特征自由搭配检测靶标圣湘生物正在下一盘大棋。通过本次获批,其“小联检”产品线扩展至8款,构建起完整的“6/3+X”呼吸道感染检测体系:这种“积木式”产品架构,让医院能够像“点菜”一样根据实际需求配置检测方案,极大提升了市场适应性。随着后疫情时代呼吸道病原体监测常态化,国内呼吸道检测市场正快速扩容。圣湘此次获批,完成了在门急诊快检、住院精准检测、公共卫生监测三大场景的全面布局。其“统一采样、统一扩增”的技术路线,显著降低了医院采购和设备投入成本,在医保控费大背景下具备明显竞争优势。虽然公司在公告中谨慎提示业绩不确定性,但结合当前呼吸道疾病流行态势和临床检测刚性需求,这批新产品有望快速放量。特别是在学校、养老院等聚集场所,快速检测产品的需求将持续旺盛。圣湘生物此次“四证连发”,不仅是企业研发实力的展示,更是我国呼吸道传染病防控能力的一次重要升级。在病原体日益复杂的今天,这种“快、准、灵”的检测方案,正成为守护公共健康的关键屏障。来源:圣湘生物公告
声明:本微信注明来源的稿件均为转载,仅用于分享,不代表平台立场,如涉及版权等问题,请尽快联系我们,我们第一时间更正,谢谢!