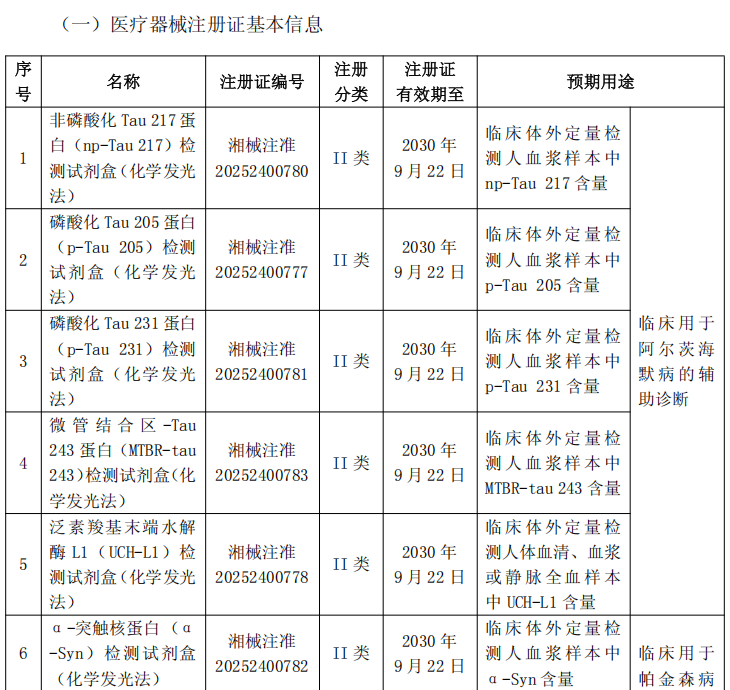
2025年9月25日,南京诺唯赞生物科技股份有限公司发布公告,其全资子公司南京诺唯赞医疗科技有限公司开发的七项神经系统系列诊断试剂产品正式获得国家药品监督管理局颁发的医疗器械注册证(II类)。
本次获批的试剂盒均采用化学发光法,覆盖阿尔茨海默病(AD)和帕金森病(PD)两大神经退行性疾病的核心生物标志物检测。具体包括:
阿尔茨海默病相关:非磷酸化Tau 217蛋白(np-Tau 217)、磷酸化Tau 205蛋白(p-Tau 205)、磷酸化Tau 231蛋白(p-Tau 231)、微管结合区-Tau 243蛋白(MTBR-tau 243)等检测试剂盒;
帕金森病相关:α-突触核蛋白(α-Syn)及其寡聚体(o-α-Syn)检测试剂盒;
脑损伤标志物:泛素羧基末端水解酶L1(UCH-L1)检测试剂盒,适用于血清、血浆或全血样本。
阿尔茨海默病与帕金森病作为全球常见的神经退行性疾病,随着人口老龄化加剧,其早期诊断与动态监测需求日益迫切。诺唯赞此次获批的产品中,多项指标为国内独家或稀缺血检标志物。例如,p-Tau217和o-α-Syn等指标在疾病早期鉴别、分期及疗效监测中具有较高临床价值。诺唯赞表示,其基于化学发光平台的AD血检解决方案已覆盖从筛查、鉴别诊断到疾病分期、预后评估的全流程,成为国内该领域获证产品数量最多的企业。在帕金森病方面,α-Syn寡聚化率(o-α-Syn/α-Syn%)的检测能力有望提升诊断特异性,区分其他α-突触核蛋白病(如路易体痴呆)。
2024年4月,诺唯赞就已有六项AD检测试剂盒获得二类医疗器械注册证,搭载化学发光平台,实现血液高灵敏检测,灵敏度可达0.5 pg/mL。
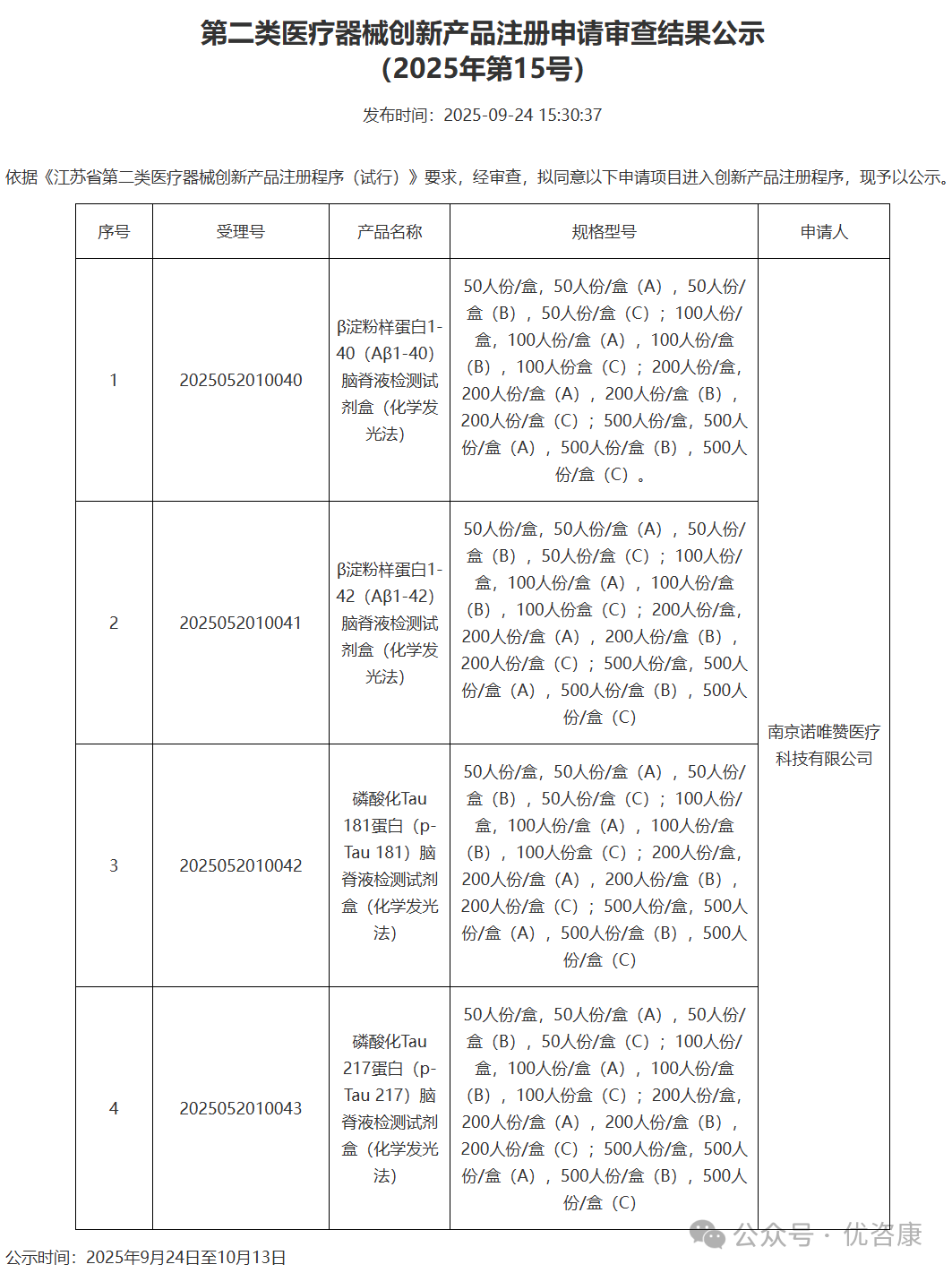
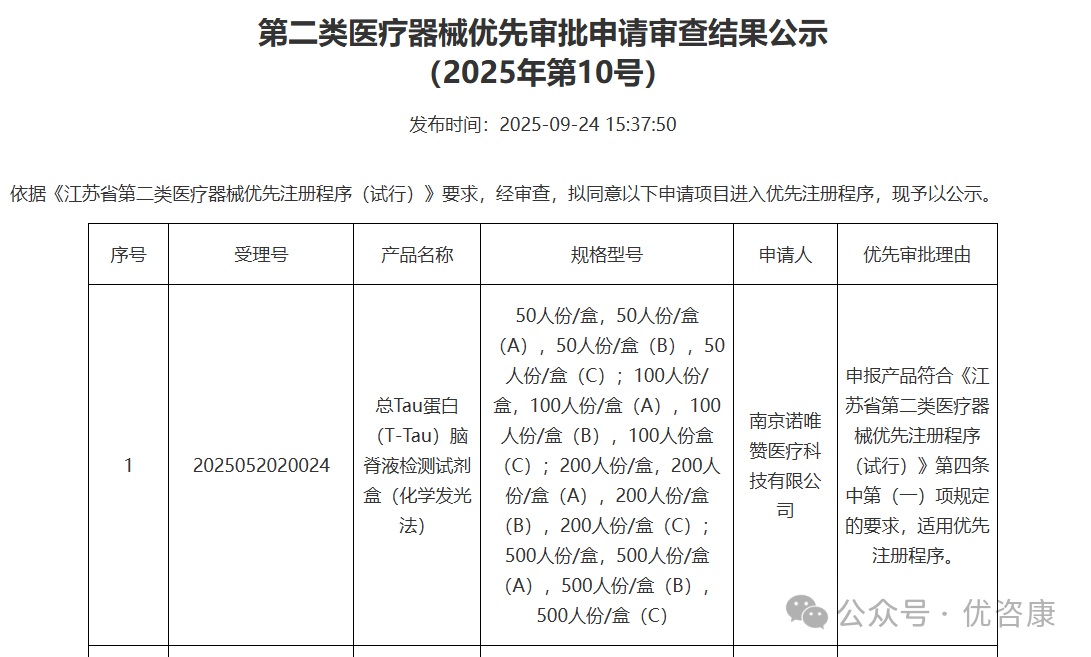
据优咨康报道,2025年9月24日,南京诺唯赞医疗科技有限公司的另外5款脑脊液AD检测试剂盒进入江苏省创新/优先审批公示。诺唯赞此次多款神经疾病血检试剂盒的集中获批,标志着我国在神经退行性疾病早期诊断领域取得重要进展。随着血检技术逐步替代传统脑脊液检测,更多患者有望获得更便捷、无创的筛查与监测手段,推动神经疾病诊疗进入精准化、可及性更高的新阶段。来源:诺唯赞公告,优咨康等
声明:该文章和信息来源于互联网,不代表本订阅号赞同其观点和对其真实性负责。如转载内容涉及版权等问题,请立即与我们联系,我们将迅速采取适当措施。